Para mis alumnos de clases particulares y para aquellos a quienes les sea útil:
Ahora que se acerca la Selectividad, voy a publicar algunos ejercicios de Selectividad resueltos para ayudaros a preparar esta prueba. Este es uno de los modelos de examen de Química del año pasado. Os sugiero que intentéis resolver el examen antes, por vuestra cuenta, en el tiempo que dura el ejercicio (1 h 30 min), y que luego comparéis la respuesta para autoevaluaros. De la corrección podréis deducir qué temas necesitáis repasar, y cuáles lleváis mejor.
Examen 121-Andalucía de Selectividad Química 2011
OPCIÓN A
1.- Formule o nombre los compuestos siguientes: a) Óxido de níquel (III) b) Hidróxido de estroncio c) Nitrobenceno d) PbBr2 e) Zn(NO2)2 f) CH2=CHCH2CH2CH3
a) Ni2O3, b) Sr(OH)2, c) C6H5-NO2 o Ph-NO2 (donde Ph denota al radical fenilo), d) bromuro de plomo (II), e) nitrito de zinc, f) pent-1-eno.
2.- a) Escriba las configuraciones electrónicas de los átomos de Na y Mg. b) Justifique por qué el valor de la primera energía de ionización es mayor para el magnesio que para el sodio. c) Justifique por qué el valor de la segunda energía de ionización es mayor para el átomo de sodio que para el de magnesio.
a) Na (Z=11): 1s2 2s2p6 3s1. Mg (Z=12): 1s2 2s2p6 3s2.
b) La energía de ionización es la energía necesaria para extraer de un átomo en estado gaseoso un electrón. En el caso del Na, la extracción de un electrón conduce a la configuración de gas noble (Na+: 1s2 2s2p6) (la configuración del Ne), con lo cual el átomo gana estabilidad química al tener la capa de valencia completamente vacía (y la anterior completamente llena); por eso no cuesta mucha energía extraer este primer electrón del Na. En cambio, en el caso del Mg la configuración resultante de la pérdida del electrón más externo no conlleva esta ganancia de estabilidad, sino que da lugar a una especie bastante inestable (Mg+:1s2 2s2p6 3s1), por tanto no es favorable energéticamente.
c) La segunda energía de ionización del Na es muy grande, porque implica la pérdida de la configuración de gas noble, de ahí que sea necesaria una gran cantidad de energía para extraer el 2º electrón del átomo (Na2+: 1s2 2s2p5). En cambio, para el Mg la situación es la contraria: la extracción del 2º electrón hace que el átomo adquiera estructura electrónica de gas noble (Mg2+: 1s2 2s2p6), con la consecuente ganancia de estabilidad, por eso es más fácil extraer el 2º electrón del Mg que el del Na.
3.- Al calentar yodo en una atmósfera de dióxido de carbono, se produce monóxido de carbono y pentóxido de diyodo, según: I2 (g) + 5CO2 (g) ↔ 5CO (g) + I2O5 (s) ∆H =1175 kJ. Justifique el efecto que tendrán los cambios que se proponen: a) Disminución del volumen sobre el valor de la constante Kc. b) Adición de I2 sobre la cantidad de CO. c) Reducción de la temperatura sobre la cantidad de CO2.
a) De acuerdo con el Principio de LeChâtelier, una disminución del volumen aumentará la presión, disminuyendo el cociente de reacción Qc ó Qp, y haciendo que el equilibrio se desplace hacia los productos (donde hay menos moles gaseosos); pero NO afecta a la constante de equilibrio. Siempre lo preguntan y es una pregunta trampa: la constante Kc sólo depende de la temperatura.
b) La adición de I2 al sistema en equilibrio hace que el sistema responda evolucionando en el sentido en que se consume I2, es decir hacia los productos. Por tanto aumenta la concentración de CO.
c) Disminuir la temperatura hará que el sistema evolucione en el sentido exotérmico (∆H <0), es decir, hacia la formación de reactivos. Por tanto aumentará la cantidad de CO2.
4.- Dada la siguiente transformación química: HC≡C-CH2-CH3 + x A → B, justifique si las siguientes afirmaciones son verdaderas o falsas: a) Cuando x = 2 y A = Cl2 el producto B presenta isomería geométrica. b) Cuando x = 1 y A = H2 el producto B presenta isomería geométrica. c) Cuando x = 1 y A = Br2 el producto B presenta isomería geométrica.
a) Falso: el 1,1,2,2-tetracloro butano carece de isomería. No puede presentar isomería geométrica porque no tiene doble enlace C=C.
b) Falso: el but-1-eno carece de isomería geométrica porque aunque tiene el doble enlace C=C, al estar éste en posición 1, el C-1 presenta dos sustituyentes iguales (H2C=CH-CH2-CH3)
c) Verdadero: el 1,2-dibromobut-1-eno sí presenta doble enlace C=C, entre carbonos con sustituyentes diferentes, lo que permite la existencia de isómeros geométricos:
isómero cis: 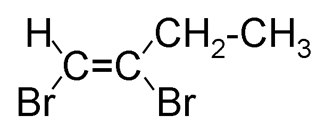 e isómero trans:
e isómero trans: 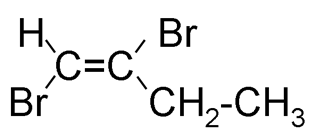
5.- A 25ºC una disolución acuosa de amoniaco contiene 0’17 g de este compuesto por litro y se encuentra disociado en un 4’3 %. Calcule: a) La concentración de iones hidroxilo y amonio. b) La constante de disociación. Masas atómicas: N = 14; H = 1.
a) La concentración de NH3 es: C=0,17g/L; en 1L hay n=0,17g/17g·mol-1 = 0,01mol NH3; por tanto la molaridad es 0,01M.
| NH3 | + | H2O | ↔ | NH4+ | + | OH– | |
| inicial |
0,01 |
– |
– |
– |
|||
| transformados |
-0,01α |
– |
+0,01α |
+0,01α |
|||
| equilibrio | 0,01(1-α) |
– |
0,01α | 0,01α |
Como α =4,3%=0,043, en el equilibrio habrá: [NH4+]=[OH–] =0,01α = 4,3·10-4 M
b) La constante Kb la obtendremos a partir de las concentraciones en el equilibrio [NH4+]=[OH–]= 0,01α = 4,3·10-4 M; [NH3]= 0,01(1- α) =0,00957M, luego:

6.- En disolución acuosa el ácido sulfúrico reacciona con cloruro de bario precipitando totalmente sulfato de bario y obteniéndose además ácido clorhídrico. Calcule: a) El volumen de una disolución de ácido sulfúrico de 1’84 g/mL de densidad y 96 % de riqueza en masa, necesario para que reaccionen totalmente 21’6 g de cloruro de bario. b) La masa de sulfato de bario que se obtendrá. Masas atómicas: H = 1; O = 16; S = 32; Ba = 137’4; Cl = 35’5.
a) Lo primero que hay que hacer en todos los problemas de estequiometría es ajustar la reacción: H2SO4 + BaCl2 → BaSO4 + 2HCl
De la reacción ajustada obtenemos la relación en moles entre el BaCl2 y el H2SO4 consumidos (1:1). Teniendo en cuenta además que el BaCl2 pesa 208,4 g/mol, el H2SO4 98 g/mol, la riqueza en peso del ácido es 96% y la densidad 1,84 g/ml:

b) La masa de BaSO4 resultante se puede calcular a partir de la reacción ajustada (1 mol BaSO4/mol BaCl2) y el peso fórmula del BaSO4 (233,4g/mol):
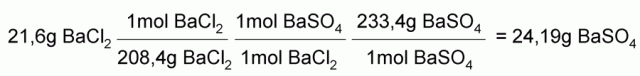
OPCIÓN B
1.- Formule o nombre los compuestos siguientes: a) Ácido hipobromoso b) Hidróxido de cobre (II) c) Ácido 2-aminopropanoico d) CaO2 e) NaHCO3 f) CH2=CHCH2CHO
a) HBrO, b) Cu(OH)2, c) CH3-CH(NH2)-COOH, d) peróxido de calcio, e) hidrógeno carbonato (IV) de sodio o bicarbonato sódico, f) but-3-enal.
2.- a) ¿Cuál es la masa, expresada en gramos, de un átomo de calcio? b) ¿Cuántos átomos de cobre hay en 2’5 g de ese elemento? c) ¿Cuántas moléculas hay en una muestra que contiene 20 g de tetracloruro de carbono? Masas atómicas: C = 12; Ca = 40; Cu = 63’5; Cl = 35’5.
a) 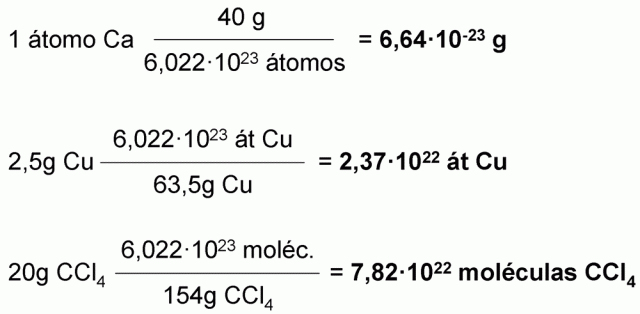
.
b)
.
c)
3.- En la tabla siguiente se indican los potenciales estándar de distintos pares en disolución acuosa
| Fe2+/Fe = −0’44 V | Cu2+/Cu= 0’34 V | Ag+/Ag = 0’80 V | Pb2+/Pb = 0’14 V | Mg2+/Mg = −2’34 V |
a) De estas especies, razone: ¿Cuál es la más oxidante? ¿Cuál es la más reductora? b) Si se introduce una barra de plomo en una disolución acuosa de cada una de las siguientes sales: AgNO3, CuSO4, FeSO4 y MgCl2, ¿en qué casos se depositará una capa de otro metal sobre la barra de plomo? Justifique la respuesta.
a) El par rédox más oxidante es el que tiene mayor tendencia a reducirse, y por tanto el de potencial normal de reducción más positivo, es decir, el par Ag+/Ag (Eº=+0,80 V). El par más reductor es el de mayor tendencia a oxidarse, o sea el que tiene el potencial de reducción más negativo, que es el Mg2+/Mg (Eº=-2,34 V).
b) Se depositará una capa de metal sobre el plomo para aquellos metales que sean capaces de oxidar al Pb (más oxidantes), o sea, para los metales que presenten un potencial de reducción más positivo que el del par Pb2+/Pb. Por tanto, se depositarán espontáneamente sobre el Pb el Cu (Eº=+0,34 V) y la Ag (Eº=+0,80 V), al sumergir la barra de plomo en las disoluciones de CuSO4 y de AgNO3, respectivamente.
4.- Al disolver en agua las siguientes sales: KCl, NH4NO3 y Na2CO3, justifique mediante las reacciones correspondientes qué disolución es: a) Ácida. b) Básica. c) Neutra.
El KCl se forma por reacción entre el HCl, que es un ácido fuerte, y el KOH, que es una base fuerte: HCl + KOH → KCl + H2O. Al disolverse esta sal, se disocia en los iones K+ y Cl–, que no se hidrolizan (dado que son el ácido conjugado de una base muy fuerte y la base conjugada de un ácido muy fuerte): KCl → K+ + Cl–, por lo que no modifican el pH del agua. Da lugar a un pH neutro, pues.
El NH4NO3 se forma por reacción entre el ácido fuerte HNO3 y la base débil NH3, según: HNO3 + NH3 → NH4NO3, y al disolverse se disocia según: NH4NO3 → NO3– + NH4+. El ion NO3– no se hidroliza, porque es la base conjugada de un ácido muy fuerte (por tanto una base muy débil), pero el NH4+, al ser el ácido conjugado de una base débil, presenta cierto carácter ácido débil, y se hidroliza según: NH4+ + H2O ↔ NH3 + H3O+. Por esta razón, esta sal da un pH ácido al disolverse en agua.
Igualmente, el Na2CO3 es la sal que forman el ácido H2CO3 (débil) y la base fuerte NaOH, según: H2CO3 + 2 NaOH → Na2CO3 + 2H2O, y se disocia en agua según: Na2CO3 → 2Na+ + CO32-. El ion Na+ no se hidroliza, porque procede de una base fuerte, pero el CO32-, al ser la base conjugada de un ácido débil, presenta carácter básico débil, hidrolizándose según: CO32- + H2O ↔ CO2 + 2OH– (en un primer paso se protona para dar ácido carbónico, y éste se descompone en CO2 y agua: CO32- + 2H2O ↔ H2CO3 + 2OH–; H2CO3 ↔ H2O + CO2). De ahí, el pH básico al disolverse esta sal en agua.
5.- La reacción utilizada para la soldadura aluminotérmica es: Fe2O3 (s) + 2Al (s) → Al2O3 (s) + 2Fe (s). a) Calcule el calor a presión constante y el calor a volumen constante intercambiados en condiciones estándar y a la temperatura de la reacción. b) ¿Cuántos gramos de Al2O3 se habrán obtenido cuando se desprendan 10000 kJ en la reacción? Datos: ΔHºf [Al2O3 (s)] = −1675’7 kJ/mol, ΔHºf [Fe2O3(s)] = −824’2 kJ/mol. Masas atómicas: Al = 27; O = 16.
a) Según el Primer Principio de la Termodinámica, el calor Q suministrado a un sistema durante un proceso termodinámico se invierte en aumentar la energía interna U del sistema y en realizar trabajo W: Q = ∆U + W. En química el trabajo realizado por un sistema se refiere generalmente al trabajo de expansión de los gases generados en una reacción, y se puede expresar como: W = p ∆V, para la expansión del gas desde un volumen inicial V0 hasta un volumen final V0+ ∆V contra una presión externa p constante.
Así, el calor intercambiado a presión constante será: Qp = ∆U + W = ∆U + p ∆V = ∆(U+pV) = ∆H, la variación de entalpía. En cambio, cuando el proceso se lleva a cabo a volumen constante, será: Qv = ∆U + W = ∆U + p ∆V = ∆U, la variación de la energía interna, dado que no se permite la expansión de los gases a V=constante. Por tanto, la relación existente entre el calor intercambiado por el sistema cuando un proceso se lleva a cabo a V=cte y el intercambiado a p=cte viene dado por: Qv = Qp – p ∆V.
Aplicado a nuestro sistema, tendremos que: Qp = ∆Hº = ∆Hºf(Al2O3) – ∆Hºf(Fe2O3) = -1675,7 + 824,2 = -851,5 kJ. Como en nuestra reacción no se generan gases, sino que todos los reactivos y productos intervienen en el estado sólido, entonces se considera que ∆V = 0, y que W = 0, por lo que Qv = Qp – p ∆V = Qp = -851,5 kJ.
b) 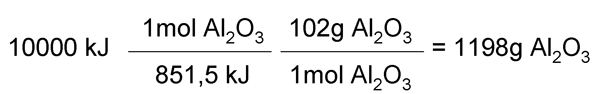
6.- En un recipiente de 2 L se introducen 2’1 mol de CO2 y 1’6 mol de H2 y se calienta a 1800 ºC. Una vez alcanzado el siguiente equilibrio: CO2 (g) + H2 (g) ↔ CO (g) + H2O (g). Se analiza la mezcla y se encuentra que hay 0’9 mol de CO2. Calcule: a) La concentración de cada especie en el equilibrio. b) El valor de las constantes Kc y Kp a esa temperatura.
a) V=2L, T=2073K. Para hallar las concentraciones de todas las especies en el equilibrio, haremos el cuadro siguiente (se indican los números de moles):
| CO2 (g) | + | H2 (g) | ↔ | CO (g) | + | H2O (g) | |
| inicial |
2,1 |
1,6 |
– |
– |
|||
| transformados |
-x |
-x |
+x |
+x |
|||
| equilibrio |
2,1-x = 0,9 |
1,6-x |
x |
x |
Si en el equilibrio la cantidad de CO2 presente son 0,9 moles, entonces la cantidad transformada de CO2 y de H2 son x=1,2 moles, y esta cantidad coincide con los moles formados de CO y de agua. Se nos pide la concentración de cada especie en el equilibrio, así que tendremos:
[CO2] = 0,9moles / 2L = 0,45M
[H2] = (1,6 – 1,2) moles / 2L = 0,4 moles / 2L = 0,2M
[CO] = [H2O] = 1,2 moles / 2L = 0,6M
b) La constante de equilibrio en función de las concentraciones Kc será:
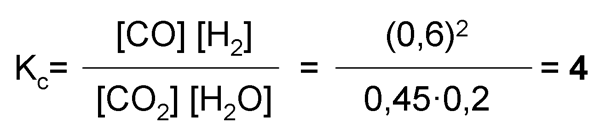
La constante en función de las presiones parciales Kp se puede obtener como sigue. Según la ecuación de los gases ideales y la Ley de Raoult, la presión parcial de un gas «i» en una mezcla p(i) es igual a la que ejercería el mismo número de moles del gas n(i) si estuviera solo en el mismo volumen, coincidiendo con el valor de la concentración molar del gas por la constante R de los gases y por la temperatura absoluta T:
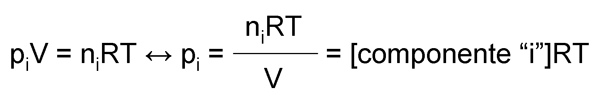
Pues llevado a la expresión de la Kp, tenemos que en general Kp = Kc RT∆n, donde ∆n denota la variación en el número de moles de gas entre los reactivos y los productos. En el caso particular de nuestra reacción, tendremos:
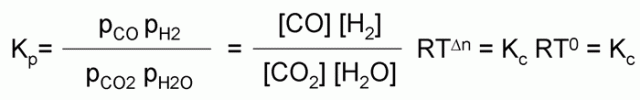
de donde, como la variación en el número de moles es ∆n=0, entonces Kp = Kc = 4.
_______________________________________
Como las fórmulas y los cálculos no se ven bien, os dejo el examen resuelto en pdf para descargar.
Descargar examen 121-Andalucía Química Selectividad 2011 resuelto

